藥明康德:從700平米實(shí)驗(yàn)室起步,到超2700億市值的醫(yī)藥外包業(yè)巨頭
2018年以來(lái),隨著一致性評(píng)價(jià)、帶量采購(gòu)等政策的出臺(tái),國(guó)內(nèi)制藥行業(yè)正面臨著一系列前所未有的挑戰(zhàn)。其中,仿制藥企業(yè)所受沖擊最大,動(dòng)輒腰斬、乃至一折的集采價(jià)格,讓部分仿制藥上市公司的估值向化工企業(yè)看齊。
與此同時(shí),創(chuàng)新藥企業(yè)則迎來(lái)政策紅利期,臨床試驗(yàn)機(jī)構(gòu)資格認(rèn)定備案制、上市許可持有人制度等利好政策紛紛落地,醫(yī)藥企業(yè)也紛紛加大對(duì)創(chuàng)新藥研發(fā)的投資。
然而,新藥研發(fā)從本質(zhì)上看并不是一門(mén)“好生意”,因?yàn)樾滤幯邪l(fā)本身的風(fēng)險(xiǎn)極高。在“雙十定律”與“專(zhuān)利懸崖”的約束下,創(chuàng)新藥面臨著投入高、周期長(zhǎng)、投資回報(bào)率越來(lái)越低的現(xiàn)實(shí)困境。盡管目前國(guó)內(nèi)二級(jí)市場(chǎng)對(duì)創(chuàng)新藥企業(yè)的業(yè)績(jī)表現(xiàn)體現(xiàn)出了很大的容忍度,但隨著太多沒(méi)有業(yè)績(jī)、沒(méi)有銷(xiāo)售收入、僅有在研項(xiàng)目的“新型藥企”登陸資本市場(chǎng),創(chuàng)新藥藥企估值的壓力恐怕遲早會(huì)體現(xiàn)出來(lái)。
相對(duì)而言,CRO(合同研究組織)則是一個(gè)更加值得關(guān)注的賽道,行業(yè)增速較高、業(yè)績(jī)更為穩(wěn)定。目前看,無(wú)論是醫(yī)藥大廠(chǎng)、還是創(chuàng)新性公司,都需要與CRO企業(yè)密切合作。從醫(yī)藥政策來(lái)看,CRO行業(yè)不受集采政策沖擊,而創(chuàng)新藥制度紅利則照單全收。
二級(jí)市場(chǎng)看,CRO企業(yè)的漲幅同樣可觀。回歸A股之后,國(guó)內(nèi)CRO龍頭企業(yè)藥明康德股價(jià)已經(jīng)從12.69元的發(fā)行價(jià)上漲至110.97元,不到三年的時(shí)間漲幅超過(guò)7倍。在股價(jià)上漲背后,是藥明康德出色的財(cái)務(wù)業(yè)績(jī)表現(xiàn),根據(jù)公開(kāi)數(shù)據(jù)顯示,藥明康德2019年全年?duì)I收為128.72億元,歸屬于母公司股東的凈利潤(rùn)為18.55億元。2020年前三季度,營(yíng)收為118.15億元,歸屬于母公司股東的凈利潤(rùn)為23.68億元,已超2019年全年。此外,創(chuàng)業(yè)板上市的CRO企業(yè)泰格醫(yī)藥股價(jià)則從2019年1月的23.92元漲至130元,兩年內(nèi)漲幅超過(guò)4倍。
作為CRO行業(yè)的龍頭,藥明康德目前在營(yíng)收規(guī)模、產(chǎn)業(yè)鏈布局以及客戶(hù)資源等方面都處于絕對(duì)領(lǐng)先的地位,值得深入研究。
由于CRO行業(yè)本身是從國(guó)外引入的一個(gè)全新的行業(yè),本文將從國(guó)外市場(chǎng)開(kāi)始回顧行業(yè)的起源與發(fā)展,這也代表著藥明康德迅速成長(zhǎng)的“天時(shí)”因素。
天時(shí):應(yīng)運(yùn)而生的CRO行業(yè)
CRO的全稱(chēng)為Contract Research Organization,是指代表客戶(hù)在藥物研發(fā)過(guò)程中負(fù)責(zé)全部或部分的科學(xué)或醫(yī)學(xué)實(shí)驗(yàn)的學(xué)術(shù)性或商業(yè)性組織。作為醫(yī)藥研發(fā)分工專(zhuān)業(yè)化和風(fēng)險(xiǎn)平均化的產(chǎn)物,CRO行業(yè)起源于醫(yī)藥產(chǎn)業(yè)最為發(fā)達(dá)的美國(guó),距今不過(guò)50年的歷史。
上個(gè)世紀(jì)60年代,隨著FDA對(duì)藥品審查的不斷趨嚴(yán),制藥企業(yè)新藥的研發(fā)成本持續(xù)攀升,甚至出現(xiàn)了著名的“雙十定律”——一款新藥從研發(fā)到上市,平均需要10年時(shí)間和10億美元的投入。而投資十年,十億美元,最后仍有可能以失敗告終。
此外,新藥上市之后,一旦過(guò)了專(zhuān)利保護(hù)期,又要面臨仿制藥的巨大沖擊,“專(zhuān)利懸崖”問(wèn)題讓創(chuàng)新藥投入回報(bào)率進(jìn)一步下滑。
面對(duì)醫(yī)藥領(lǐng)域投資這個(gè)“雙十定律”的屬性以及“專(zhuān)利懸崖”的困境,一些大型藥企開(kāi)始將醫(yī)藥研發(fā)的部分環(huán)節(jié)進(jìn)行剝離并外包給更為專(zhuān)業(yè)的組織機(jī)構(gòu),這就促使了合同研究組織(CRO)行業(yè)的應(yīng)運(yùn)而生。
相對(duì)而言,合同研究組織更加專(zhuān)注于新藥研發(fā)流程中的一個(gè)或者幾個(gè)環(huán)節(jié),專(zhuān)業(yè)水平高、研發(fā)周期縮短,大大提升了研發(fā)效率。而對(duì)于藥企來(lái)說(shuō),中間環(huán)節(jié)外包不僅可以收窄自身業(yè)務(wù)、聚焦更為關(guān)鍵的領(lǐng)域,還可以分散整個(gè)醫(yī)藥研發(fā)流程中的風(fēng)險(xiǎn)。
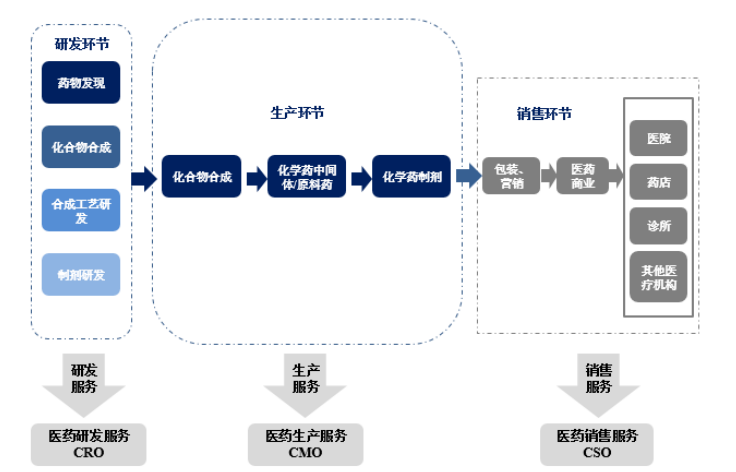
一款新藥從研發(fā)到上市大致要分為藥物發(fā)現(xiàn)、臨床前研究、臨床研究、注冊(cè)審批等階段,而每一個(gè)環(huán)節(jié)又有很多細(xì)分。如果藥企進(jìn)行獨(dú)立研發(fā),任何一個(gè)環(huán)節(jié)出錯(cuò)都可能出現(xiàn)前功盡棄的狀況。因此,借助于CRO就可以降低藥企自身的投資壓力與系統(tǒng)風(fēng)險(xiǎn),并可以將自身精力聚焦于疾病機(jī)理研究及新藥靶點(diǎn)的發(fā)現(xiàn)等核心研發(fā)業(yè)務(wù)。
20世紀(jì)80年代,越來(lái)越多的美國(guó)藥企開(kāi)始將部分工作轉(zhuǎn)移給CRO企業(yè)完成,CRO行業(yè)迎來(lái)了快速發(fā)展期。此外,輕資產(chǎn)運(yùn)營(yíng)的Biotech藥企不斷崛起,同樣促進(jìn)了CRO行業(yè)的繁榮。對(duì)于大部分小型和虛擬創(chuàng)新型藥來(lái)說(shuō),都存在資金設(shè)備以及人力不足的問(wèn)題,與CRO合作就成為順理成章的事情。
目前,作為醫(yī)藥服務(wù)類(lèi)行業(yè),CRO主要有客戶(hù)定制服務(wù)(Fee-For-Sevice,F(xiàn)FS)及全時(shí)當(dāng)量服務(wù)(Full-Time Equivalent,F(xiàn)TE)兩種收費(fèi)模式。在客戶(hù)定制服務(wù)模式下,CRO企業(yè)一般基于單項(xiàng)合約、里程碑或者研發(fā)季度,在履行義務(wù)得以滿(mǎn)足時(shí)確認(rèn)收入。如此一來(lái),無(wú)論試驗(yàn)結(jié)果成功與否,只要數(shù)據(jù)準(zhǔn)確,化合物達(dá)到要求,CRO企業(yè)都能收取既定的服務(wù)費(fèi)。
在全時(shí)當(dāng)量服務(wù)模式下,CRO公司會(huì)將實(shí)驗(yàn)人員分配給客戶(hù)進(jìn)行合同約定的研究項(xiàng)目,根據(jù)記錄的實(shí)際工時(shí)乘以合同約定的全時(shí)當(dāng)量勞務(wù)費(fèi)率確認(rèn)收入。
因此,無(wú)論是FFS模式還是FTE模式,CRO公司都不需要對(duì)試驗(yàn)結(jié)果“負(fù)責(zé)”,CRO業(yè)務(wù)模式就具有了旱澇保收的特征,這一優(yōu)勢(shì)是全球CRO行業(yè)得以快速發(fā)展的一個(gè)重要原因。
地利:高速增長(zhǎng)的中國(guó)市場(chǎng)
20世紀(jì)90年代,大型藥企開(kāi)始加速業(yè)務(wù)的全球化布局,并在海外市場(chǎng)設(shè)立研發(fā)分支機(jī)構(gòu)。這既加速了CRO行業(yè)的發(fā)展,又帶動(dòng)了CRO產(chǎn)業(yè)向發(fā)展中國(guó)家的轉(zhuǎn)移。
1996年,美國(guó)國(guó)際研發(fā)外包服務(wù)企業(yè)MDS Pharma Service在我國(guó)投資設(shè)立了國(guó)內(nèi)第一家真正意義上的合同研究公司,從事新藥的臨床試驗(yàn)業(yè)務(wù)。隨后,美國(guó)Quintiles(昆泰)、科文斯等行業(yè)巨頭也紛紛在中國(guó)成立分支機(jī)構(gòu),帶動(dòng)了中國(guó)CRO產(chǎn)業(yè)的發(fā)展。
2000年之后,藥明康德、泰格醫(yī)藥、博濟(jì)醫(yī)藥等公司相繼成立,代表著本土CRO企業(yè)的興起。其中,藥明康德發(fā)展最為迅速,公司最早只有700平方米實(shí)驗(yàn)室,如今已經(jīng)成為全球CRO行業(yè)的龍頭企業(yè)之一。高速發(fā)展的中國(guó)市場(chǎng),為公司的崛起提供了“地利”之便。
根據(jù)全國(guó)醫(yī)藥技術(shù)市場(chǎng)協(xié)會(huì)的統(tǒng)計(jì)數(shù)據(jù),2013年-2018年,我國(guó)CRO市場(chǎng)規(guī)模從231億元迅速增長(zhǎng)到678億元,年均復(fù)合增長(zhǎng)率達(dá)到24.03%,成為全球CRO行業(yè)增速最快的市場(chǎng)。
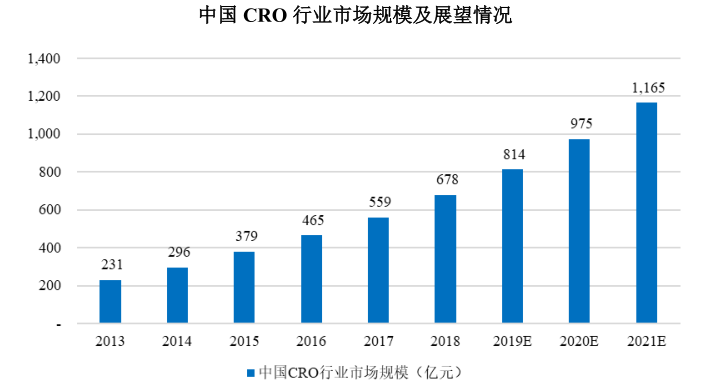
除了行業(yè)起步晚、基數(shù)較低這一原因外,創(chuàng)新藥的興起、仿制藥的壓力以及研發(fā)服務(wù)外包滲透率的持續(xù)提升也是中國(guó)CRO市場(chǎng)增速領(lǐng)先全球的重要原因。
首先,隨著國(guó)家醫(yī)藥政策的改革以及對(duì)創(chuàng)新藥物研發(fā)的鼓勵(lì),國(guó)內(nèi)醫(yī)藥行業(yè)“重銷(xiāo)售、輕研發(fā)”的境況有所好轉(zhuǎn),國(guó)內(nèi)制藥企業(yè)對(duì)于研發(fā)領(lǐng)域的投入持續(xù)增加。
過(guò)去很長(zhǎng)一段時(shí)期,我國(guó)新藥審批較為緩慢,同一種新藥批準(zhǔn)上市時(shí)間要比美國(guó)晚上5年以上。自2014年以來(lái),隨著臨床試驗(yàn)機(jī)構(gòu)資格認(rèn)定備案制、上市許可持有人制度等藥品政策紛紛落地,新藥研發(fā)的制度紅利促進(jìn)了國(guó)內(nèi)藥企對(duì)新藥研發(fā)的投入。
2019年,百濟(jì)神州抗癌藥“澤布替尼”成功在美國(guó)上市,成為中國(guó)首款獲得FDA批準(zhǔn)的創(chuàng)新藥,國(guó)內(nèi)新藥研發(fā)取得了階段性成果。與此同時(shí),以百濟(jì)神州、君實(shí)生物等為代表新型創(chuàng)新藥企日益受到資本的重視,融資狀況大為好轉(zhuǎn),而這些新型Biotech公司正是醫(yī)藥研發(fā)外包服務(wù)的重要需求方。
Frost&Sullivan數(shù)據(jù)顯示,2014-2019年,我國(guó)醫(yī)藥研發(fā)投入由93億美元增長(zhǎng)至216億美元,年均復(fù)合增長(zhǎng)率達(dá)到18.6%,醫(yī)藥行業(yè)研發(fā)投入的較快增長(zhǎng)構(gòu)成了國(guó)內(nèi)CRO產(chǎn)業(yè)快速發(fā)展的基本盤(pán)。
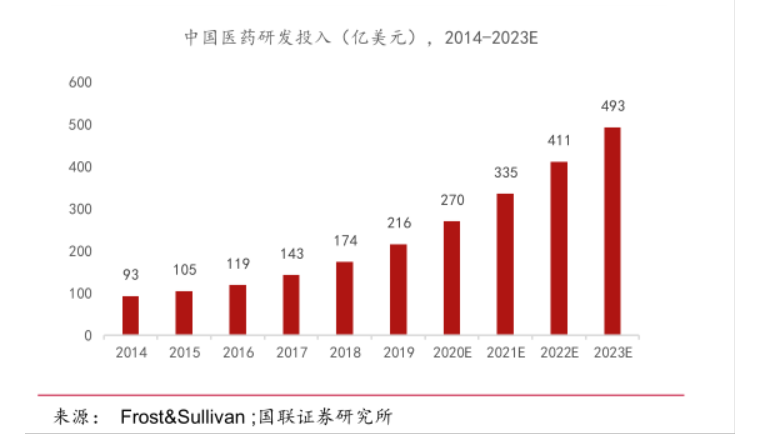
隨著國(guó)內(nèi)CRO市場(chǎng)的逐步發(fā)展,國(guó)內(nèi)制藥公司也很快意識(shí)到與CRO合作可以提高新藥研發(fā)效率、縮短臨床時(shí)間。因而,與全球市場(chǎng)一樣,國(guó)內(nèi)CRO行業(yè)同樣受益于滲透率的提升,行業(yè)增速持續(xù)超過(guò)同期醫(yī)藥投入增長(zhǎng)水平。
數(shù)據(jù)顯示,2014年至2018年,全球CRO市場(chǎng)規(guī)模由380億美元增長(zhǎng)至550億美元,銷(xiāo)售額年復(fù)合增速為9.6%,而同期全球醫(yī)藥研發(fā)投入增速為5.2%,滲透率的提升是CRO行業(yè)始終保持較高增速的一個(gè)關(guān)鍵因素。
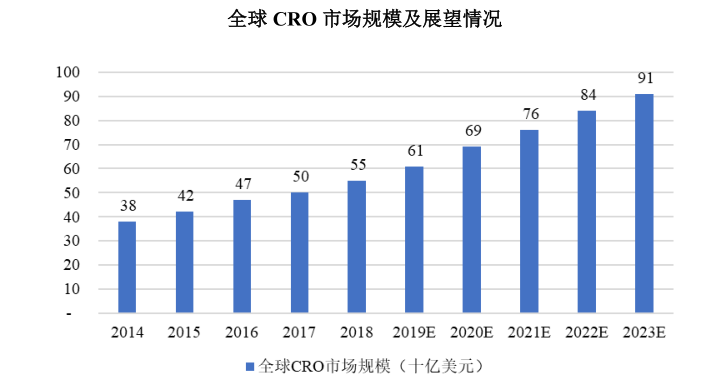
前文已經(jīng)提及,CRO企業(yè)不僅以高效贏得了大型藥企的業(yè)務(wù)訂單,還通過(guò)彌補(bǔ)小型藥企研發(fā)能力不足的優(yōu)勢(shì),進(jìn)一步擴(kuò)大了CRO產(chǎn)業(yè)的服務(wù)范圍。
統(tǒng)計(jì)數(shù)據(jù)顯示,目前超過(guò)50%的制藥企業(yè)都開(kāi)始與CRO合作。從全球市場(chǎng)來(lái)看,CRO行業(yè)的滲透率已經(jīng)超過(guò)30%,到2022年預(yù)計(jì)將進(jìn)一步提升至37.5%。
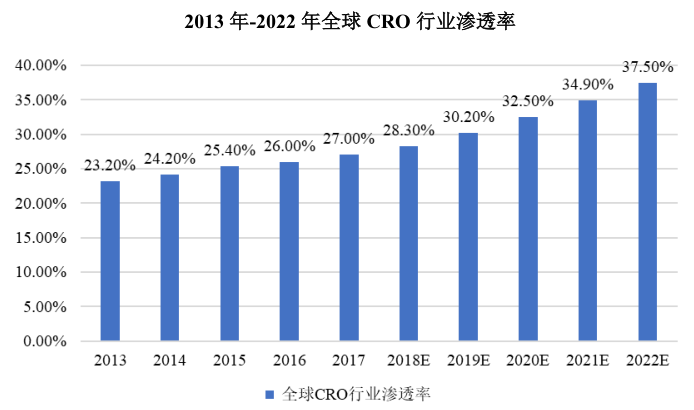
值得關(guān)注的是,隨著藥審政策的不斷趨嚴(yán),國(guó)內(nèi)仿制藥企業(yè)開(kāi)始面臨一致性評(píng)價(jià)等政策壓力,這讓研發(fā)能力較弱的仿制藥生產(chǎn)企業(yè)也加大了研發(fā)投入。因此,除了創(chuàng)新藥這一因素外,仿制藥企業(yè)對(duì)CRO需求同樣在快速增長(zhǎng),這又進(jìn)一步促進(jìn)了國(guó)內(nèi)CRO行業(yè)的發(fā)展。
數(shù)據(jù)顯示,2019年全球醫(yī)藥市場(chǎng)規(guī)模約為1.23萬(wàn)億美元,其中中國(guó)醫(yī)藥市場(chǎng)規(guī)模約1.7萬(wàn)億元人民幣,占比約為20%。同期,2019年全球CRO市場(chǎng)規(guī)模約為626億美元,中國(guó)市場(chǎng)為63億美元,占比僅為10%。對(duì)比來(lái)看,我國(guó)CRO市場(chǎng)占全球的比重仍然較低。
Frost&Sullivan研究報(bào)告顯示,2023年全球CRO規(guī)模將達(dá)到877億美元,其中中國(guó)CRO市場(chǎng)規(guī)模將會(huì)達(dá)到172億美元,占全球規(guī)模將提升到20%。由此來(lái)看,國(guó)內(nèi)CRO行業(yè)未來(lái)仍然有較大提升空間。
人和:工程師紅利促進(jìn)了藥明康德的崛起
由于CRO行業(yè)具有“勞動(dòng)密集型”的特征,國(guó)內(nèi)工程師紅利所帶來(lái)的成本優(yōu)勢(shì)也成為中國(guó)CRO快速發(fā)展的又一重要因素。數(shù)據(jù)顯示,國(guó)內(nèi)藥企研發(fā)崗位的入職年薪約為發(fā)達(dá)國(guó)家的四分之一,中國(guó)人力成本優(yōu)勢(shì)非常突出。
此外,由于臨床CRO業(yè)務(wù)需要招募患者進(jìn)行參與,我國(guó)龐大的人口基數(shù)決定了患者招募成本低,效率也遠(yuǎn)高于發(fā)達(dá)國(guó)家。因此,越來(lái)越多的國(guó)際制藥企業(yè)選擇在中國(guó)開(kāi)展臨床,全球CRO產(chǎn)業(yè)開(kāi)始向中國(guó)轉(zhuǎn)移。
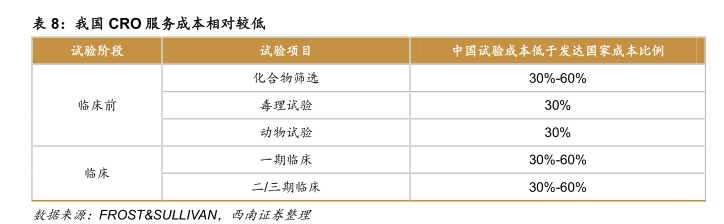
作為本土企業(yè)來(lái)說(shuō),藥明康德人力成本僅相當(dāng)于外資CRO巨頭的三分之一,這對(duì)于人力密集型的CRO行業(yè)至關(guān)重要。換個(gè)角度來(lái)看,CRO行業(yè)誕生的意義就在于降低新藥研發(fā)的整體成本。因此,人力成本優(yōu)勢(shì)已經(jīng)成為本土CRO迅速發(fā)展并壯大的核心競(jìng)爭(zhēng)力。
藥明康德的創(chuàng)始人李革出生于北京,北大化學(xué)系畢業(yè)后赴美留學(xué)。在哥倫比亞大學(xué)有機(jī)化學(xué)專(zhuān)業(yè)讀博期間,李革與導(dǎo)師共同發(fā)明了“標(biāo)記的組合化學(xué)技術(shù)”,并由此發(fā)現(xiàn)了多種藥物前體化合物。作為新藥研發(fā)的重要環(huán)節(jié),這一成果讓他們順利拿到風(fēng)險(xiǎn)投資,并一起創(chuàng)辦了組合化學(xué)公司Pharmacopeia。1995年,Pharmacopeia公司成功在納斯達(dá)克上市,這一年李革僅28歲。
1999年,李革應(yīng)北大邀請(qǐng)回國(guó)訪(fǎng)問(wèn),看到了中國(guó)醫(yī)藥市場(chǎng)的機(jī)會(huì),李革決定回國(guó)創(chuàng)業(yè)。2000年12月,藥明康德正式成立,公司最早僅有700平方米的實(shí)驗(yàn)室。
在公司成立早期,國(guó)內(nèi)醫(yī)藥企業(yè)對(duì)于“研發(fā)外包服務(wù)”還非常陌生,藥明康德只能去爭(zhēng)取美國(guó)公司的訂單。由于李革在Pharmacopeia工作期間曾擔(dān)任科研和管理職位,并主導(dǎo)了多項(xiàng)與美國(guó)各大制藥公司的合作項(xiàng)目,藥明康德逐步打開(kāi)了美國(guó)市場(chǎng)。
2005年,也就是公司成立5年之后,藥明康德化學(xué)服務(wù)規(guī)模就做到了全球第一,大型制藥企業(yè)客戶(hù)資源超過(guò)80家,包括輝瑞、禮來(lái)、諾華等全球排名前十位的巨頭藥企。
2007年8月,藥明康德成功在美國(guó)紐約交易所上市,總市值突破了10億美元,并成為中國(guó)內(nèi)地藥品研發(fā)服務(wù)外包赴美上市第一股。
2015年12月,藥明康德從美股私有化退市。此后,公司拆為三大類(lèi)業(yè)務(wù)分別上市。
2018年,主營(yíng)業(yè)務(wù)為小分子化學(xué)藥發(fā)現(xiàn)、研發(fā)及生產(chǎn)的藥明康德在上交所主板上市。公司招股說(shuō)明書(shū)數(shù)據(jù)顯示,2016年藥明康德全球市場(chǎng)份額達(dá)到2.02%,排名全球第10位,中國(guó)第1位。
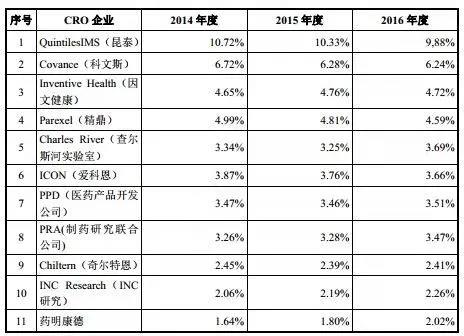
回顧藥明康德的發(fā)展,公司之所以能從一家700平方米的實(shí)驗(yàn)室成長(zhǎng)為全球CRO行業(yè)排名前十的巨頭公司,得益于創(chuàng)始人的技術(shù)實(shí)力與人脈資源之外,國(guó)內(nèi)工程師紅利也是一個(gè)重要因素,這兩者共同構(gòu)成了藥明康德在“人和”方面的優(yōu)勢(shì)。
藥明康德的四大核心競(jìng)爭(zhēng)優(yōu)勢(shì)
回歸A股之后,藥明康德業(yè)績(jī)保持了穩(wěn)定的增長(zhǎng)。數(shù)據(jù)顯示,2015-2019年,藥明康德?tīng)I(yíng)收增速分別為18%、25%、27%、24%和34%,整體處于提升趨勢(shì),顯示出公司良好的成長(zhǎng)性與綜合競(jìng)爭(zhēng)力。
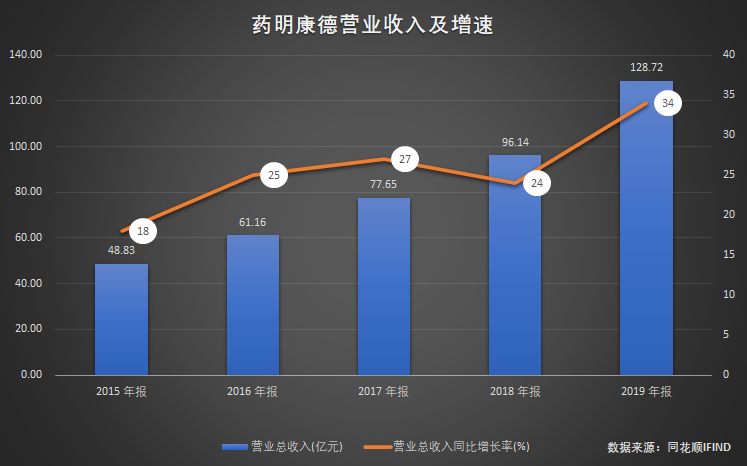
與此同時(shí),公司股價(jià)也受到資本追捧。截至12月14日,公司股價(jià)收于113.2元,市值高達(dá)2764億元,較發(fā)行價(jià)上漲超過(guò)7倍。
對(duì)比國(guó)內(nèi)同行來(lái)看,藥明康德在企業(yè)規(guī)模、產(chǎn)業(yè)鏈覆蓋度、客戶(hù)資源等方面優(yōu)勢(shì)明顯;對(duì)比外資CRO而言,藥明康德則具有明顯的本土化優(yōu)勢(shì)。
首先,藥明康德規(guī)模優(yōu)勢(shì)較為突出。作為國(guó)內(nèi)CRO行業(yè)龍頭,藥明康德2019年實(shí)現(xiàn)收入128.72億元,遠(yuǎn)超過(guò)第二梯隊(duì)的康龍化成的37.6億元和泰格醫(yī)藥的28.0億元,而藥石科技、昭衍新藥、美迪西等第三梯隊(duì)企業(yè)營(yíng)收則不足10億元。
其次,藥明康德產(chǎn)業(yè)鏈一體化優(yōu)勢(shì)明顯,尤其在臨床前CRO這一環(huán)節(jié)優(yōu)勢(shì)較為突出。
根據(jù)新藥研發(fā)生產(chǎn)的階段劃分,CRO行業(yè)又可以細(xì)分為臨床前CRO、臨床CRO、CMO/CDMO(醫(yī)藥外包生產(chǎn))三個(gè)環(huán)節(jié)。其中,臨床前CRO服務(wù)包括藥代動(dòng)力學(xué)、藥理毒理學(xué)、動(dòng)物模型等方面,臨床CRO服務(wù)主要包括臨床試驗(yàn)技術(shù)服務(wù)、數(shù)據(jù)管理、統(tǒng)計(jì)分析以及注冊(cè)申請(qǐng)四個(gè)方面;CMO/CDMO是主要負(fù)責(zé)藥品的生產(chǎn),生產(chǎn)工藝的研發(fā)升級(jí)。
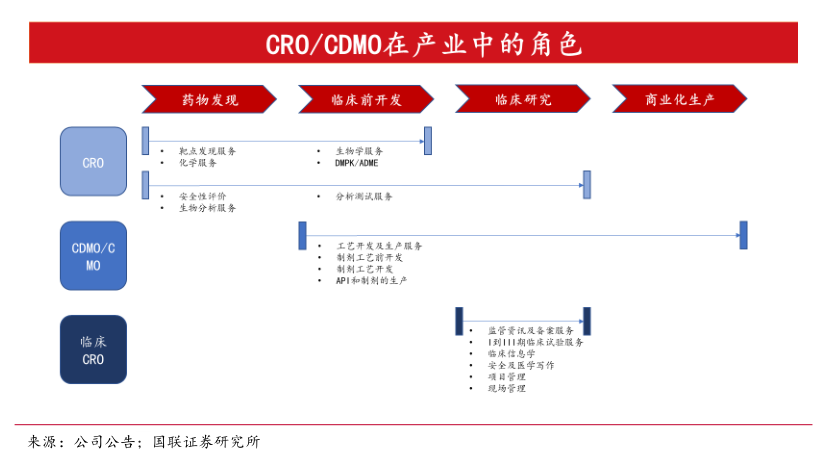
由于醫(yī)藥研發(fā)環(huán)節(jié)的技術(shù)差異性很大,國(guó)內(nèi)多數(shù)CRO公司通常專(zhuān)注于某單個(gè)或幾個(gè)環(huán)節(jié)的研究。藥明康德則具有明顯的全產(chǎn)業(yè)鏈一體化優(yōu)勢(shì),尤其在臨床前CRO這一領(lǐng)域競(jìng)爭(zhēng)力最為突出。
目前,藥明康德主營(yíng)業(yè)務(wù)共分為中國(guó)區(qū)實(shí)驗(yàn)室服務(wù)、合同生產(chǎn)研發(fā)/合同生產(chǎn)服務(wù)(CDMO/CMO)、美國(guó)區(qū)實(shí)驗(yàn)室服務(wù)、臨床研究及其他CRO服務(wù)四大類(lèi)。其中,中國(guó)區(qū)實(shí)驗(yàn)室服務(wù)主要提供臨床前的化學(xué)和生物研究服務(wù),2019年?duì)I業(yè)收入達(dá)到64.73億元,收入占比達(dá)到50.37%。
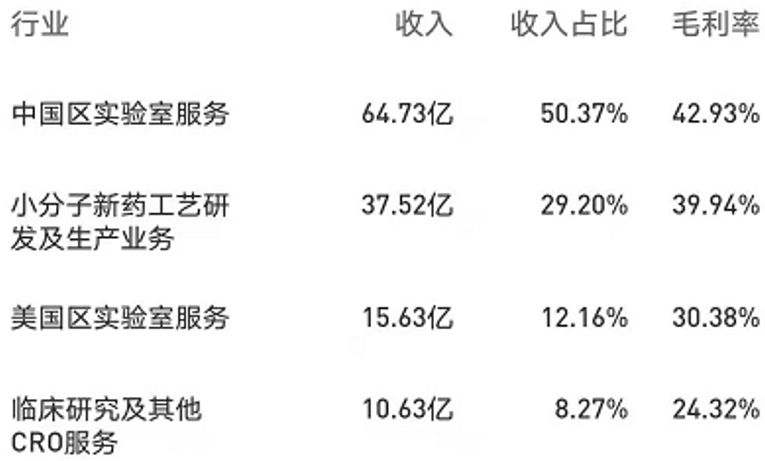
由于公司創(chuàng)始人團(tuán)隊(duì)的專(zhuān)業(yè)技術(shù)背景,藥明康德自成立以來(lái)就專(zhuān)注于臨床前CRO領(lǐng)域,公司小分子化學(xué)藥的發(fā)現(xiàn)、研發(fā)和生產(chǎn)服務(wù)十分成熟,市場(chǎng)占有率位居全球第二位。
2014年以前,藥明康德小分子藥物發(fā)現(xiàn)業(yè)務(wù)主要來(lái)自國(guó)際巨頭。2015年開(kāi)始,仿制藥的壓力和創(chuàng)新藥的紅利持續(xù)推動(dòng)國(guó)內(nèi)藥企創(chuàng)新轉(zhuǎn)型,國(guó)內(nèi)市場(chǎng)開(kāi)始迎來(lái)快速增長(zhǎng)期。與此同時(shí),藥明康德也將自身業(yè)務(wù)不斷向產(chǎn)業(yè)鏈下游擴(kuò)展,公司臨床CRO服務(wù)正在快速發(fā)展。此外,公司還通過(guò)美國(guó)區(qū)實(shí)驗(yàn)室在境外提供醫(yī)療器械檢測(cè)及細(xì)胞和基因治療的研發(fā)生產(chǎn)服務(wù)。
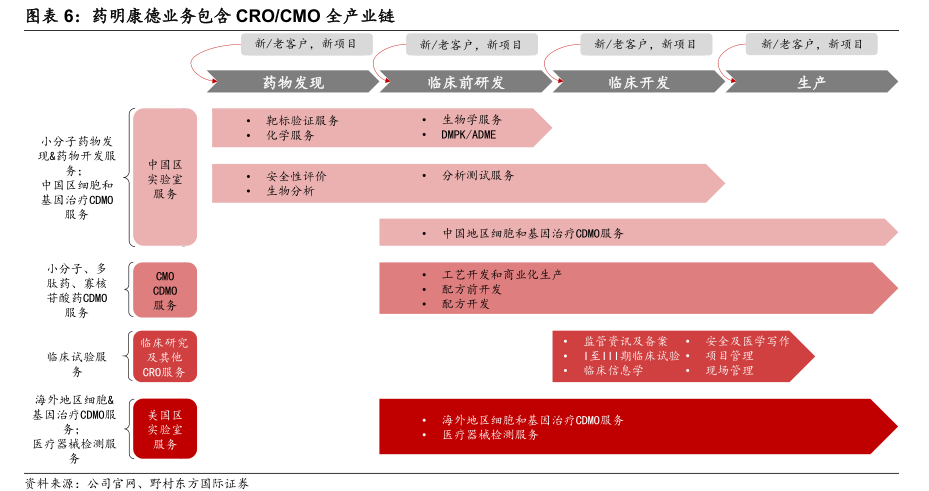
經(jīng)過(guò)多年發(fā)展,藥明康德通過(guò)全產(chǎn)業(yè)鏈布局實(shí)現(xiàn)了“一體化、端到端”的服務(wù),相比國(guó)內(nèi)企業(yè),公司的臨床前CRO和CDMO業(yè)務(wù)均為絕對(duì)龍頭,臨床CRO業(yè)務(wù)也在快速推進(jìn),全產(chǎn)業(yè)鏈布局優(yōu)勢(shì)顯著。這既增強(qiáng)了客戶(hù)粘性,也提升了業(yè)務(wù)的協(xié)同效應(yīng)。
目前,藥明康德客戶(hù)群體遍布全球,涵蓋了所有全球前20大制藥企業(yè)。近三年,公司的前十大客戶(hù)保留率均為100%。截至2020年6月30日,公司擁有4000+的活躍客戶(hù),2020年上半年新增客戶(hù)超過(guò)600家,因此,龐大且忠誠(chéng)的客戶(hù)資源優(yōu)勢(shì)成為藥明康德又一核心優(yōu)勢(shì)。
此外,相對(duì)制藥大廠(chǎng)而言,小型制藥公司新藥研發(fā)效率較高,發(fā)展較為迅速。數(shù)據(jù)顯示,2013-2017年期間,小型制藥公司獲得美國(guó)食品藥品管理局(FDA)批準(zhǔn)新藥(NDA及BLA)的比例已從7%提高到39%,預(yù)期2022年還將提高到47%。
為此,藥明康德針對(duì)這一趨勢(shì)實(shí)施了“長(zhǎng)尾戰(zhàn)略”。數(shù)據(jù)顯示,2019年公司已經(jīng)有3900多家活躍客戶(hù),新增客戶(hù)1200家。近幾年,公司海外“長(zhǎng)尾客戶(hù)”和國(guó)內(nèi)客戶(hù)的合計(jì)占比持續(xù)增長(zhǎng),已經(jīng)從2016年的59.6%提高到2019年的67.5%,充分享受了中小藥企高成長(zhǎng)紅利。
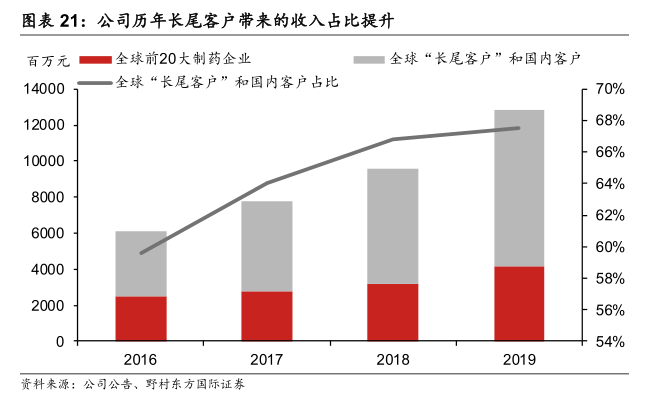
相對(duì)于跨國(guó)CRO,藥明康德臨床資源豐富、熟悉國(guó)內(nèi)臨床體制以及服務(wù)能力更強(qiáng),具有明顯的本土化及性?xún)r(jià)比優(yōu)勢(shì),這也是公司在國(guó)內(nèi)市場(chǎng)的又一大核心競(jìng)爭(zhēng)力。此外,國(guó)外大型CRO企業(yè)通常不涉及CMO業(yè)務(wù),藥明康德的產(chǎn)業(yè)鏈一體化優(yōu)勢(shì)同樣明顯。
整體來(lái)看,藥明康德在全球視野與布局、新藥研發(fā)平臺(tái)打造、客戶(hù)資源以及本土化等領(lǐng)域相對(duì)優(yōu)勢(shì)突出。與此同時(shí),公司“一站式研發(fā)平臺(tái)”也降低了新藥研發(fā)門(mén)檻,釋放了中國(guó)創(chuàng)新藥研發(fā)活力,提升了中國(guó)新藥研發(fā)的效率與競(jìng)爭(zhēng)力。因此,藥明康德雖然不直接研發(fā)新藥,卻對(duì)中國(guó)創(chuàng)新藥研發(fā)水平的提高起著推動(dòng)作用。無(wú)論是從方興未艾的創(chuàng)新藥行業(yè)分析,還是從高速增長(zhǎng)的CRO賽道考慮,藥明康德未來(lái)發(fā)展都非常值得期待。
猜你喜歡
【財(cái)報(bào)透視】三季報(bào)多項(xiàng)紀(jì)錄創(chuàng)新高,股價(jià)卻跌破百元:藥明康德遭遇“減持魔咒”?
股東減持也拖累了藥明康德的股價(jià)。利潤(rùn)大增,單季營(yíng)收破百億,藥明康德已經(jīng)成為全球創(chuàng)新藥鏈條上的關(guān)鍵企業(yè)
從在手訂單來(lái)看,藥明康德業(yè)績(jī)?cè)鲩L(zhǎng)的勢(shì)頭有望進(jìn)一步持續(xù)。藥明康德被海外“狙擊”后,來(lái)自美國(guó)的收入還漲了7.6%
藥明康德前三季度總體營(yíng)收同比下降6.23%。藥明系“狂奔”,批量生產(chǎn)IPO
巔峰時(shí)期,“藥明系”上市公司總市值曾達(dá)萬(wàn)億。



 博望財(cái)經(jīng)
博望財(cái)經(jīng)
 礪石商業(yè)評(píng)論
礪石商業(yè)評(píng)論
 野馬財(cái)經(jīng)
野馬財(cái)經(jīng)


 獵云網(wǎng)
獵云網(wǎng)



